- EN
- FR
- EN
- FR

Envoyer un échantillon/une souche au CNR des Méningocoques et Haemophilus influenzae
Attention, pour tout envoi biologique (souche ou prélèvement en vue d'une PCR), merci de remplir et joindre la fiche de renseignements.
Voici la fiche technique pour l'envoi des souches vers le CNRMHi.
Espèces du genre Neisseria autre que N. meningitidis et Haemophilus autre que H. influenzae
Leur identification bactériologique, toujours indispensable pour les différencier des espèces pathogènes, pose des problèmes de par leur difficulté de croissance et le peu de caractères phénotypiques utilisables. Le CNRMHi accepte de réaliser ce type d’identification si la souche est accompagnée d’une fiche de renseignements, et est envoyée dans les mêmes conditions de transport et d’emballage que pour le méningocoque ou H. influenzae (contacter le CNRMHi).
RECOMMANDATIONS POUR LE PRÉLÈVEMENT ET CONDITIONS PRE-ANALYTIQUES
Attention, pour tout envoi biologique (souche ou prélèvement en vue d'une PCR), merci de remplir et joindre la fiche de renseignements.
IDENTIFICATION PAR PCR EN TEMPS RÉEL
L'extrême sensibilité de la PCR impose que l'échantillon ait été prélevé, conditionné et soit transporté selon des procédures évitant toute contamination exogène (un tube récupéré après avoir subi des manipulations non stériles est absolument proscrit).
- Le LCR ainsi que d'autres fluides biologiques, tels que le liquide de ponction articulaire ou péricardique, (≥200 μl), doivent être acheminés dans un tube stérile en plastique, avec capuchon étanche, et ne doivent pas avoir été manipulés (contaminés).
- Les prélèvements sanguins (2 ml) doivent être recueillis dans un tube EDTA stérile et ne doivent pas avoir été manipulés (contaminés).
- En présence de lésions cutanées purpuriques, la PCR peut être réalisée sur la biopsie cutanée ou le produit d’aspiration des lésions. La biopsie doit être recueillie dans un tube sec stérile en plastique et ne doit pas avoir été manipulée (contaminée).
- Les échantillons destinés à la réalisation de la PCR peuvent être envoyés à -20°C, à 4°C ou à température ambiante.
- Si la PCR réalisée par l’hôpital est positive pour le méningocoque, un aliquot d’extrait d’ADN (volume > 30 μl) doit être envoyé au CNR pour un génotypage complet.
Utilisation des prélèvements biologiques pour des fins diagnostiques dans la recherche sur la physiopathologie des infections invasives à méningocoque et Haemophilus influenzae :
> Fiche de renseignements à joindre à tout envoi de PCR
> Attestation de non-opposition patient
|
Type d’échantillon |
Milieu de transport |
T°C de transport |
Délai d’acheminement |
Délai de rendu de résultat |
Informations spécifiques (ex : conditions de transport) |
|
|
|
Souche isolée |
N. meningitidis |
Écouvillon avec gel Amies Charcoal |
T° ambiante |
24-48h |
3-4j |
Envoi de matériel biologique |
|
|
H. influenzae |
Chocolat Polyvitex ou Müller-Hinton |
T° ambiante |
24-48h |
3-4j |
Envoi de matériel biologique |
||
|
Prélèvement primaire humain |
|
-20°C, 4°C ou T° ambiante |
24-48h |
≤24h si non diagnostiqué et ≤7 jours pour les confirmations |
Envoi de matériel biologique |
|
|
|
Extrait ADN issu d’un prélèvement primaire humain |
|
-20°C, 4°C ou T° ou ambiante |
24-48h |
24h si non diagnostiqué et 7 jours pour les confirmations |
Envoi de matériel biologique |
|
|
ETAT PHYSIOLOGIQUE DES SOUCHES
- Les Neisseria et Haemophilus ne restent viables que 48h dans une étuve sans repiquage sur les milieux appropriés. Attention à ne pas laisser les souches plus de 2 heures en dehors de l’étuve. Ne jamais les stocker au froid.
- Un milieu de transport, quel qu’il soit, ne peut être efficace que s’il est ensemencé avec des bactéries viables (culture de 18 à 24 heures).
Fiche de renseignements à joindre obligatoirement à tout envoi de souches.
Cette fiche doit impérativement accompagner chaque envoi de souche au CNRMHi, y compris lors de réexpédition d’une souche n’ayant pas donné de subculture. Chaque nouvel envoi étant considéré comme indépendant est enregistré comme tel (rappeler qu’il s’agit d’un nouvel envoi).
Milieu de transport adapté aux Neisseria et H. influenzae
Le milieu adapté au transport des souches de Neisseria est l'écouvillon avec gel Amies Charcoal. Il doit être ensemencé largement avec une culture pure de 18 à 24 heures maximum et incubé une nuit à 37°C dans une atmosphère enrichie en 5% CO2 avant d’être acheminé au CNRMHi à température ambiante.
Rappel : le CNRMHi fournit gratuitement ce milieu adapté sur simple demande par email à l’adresse : meningo@pasteur.fr.
Le milieu adapté au transport des souches de H. influenzae est le milieu Chocolat Polyvitex (dit milieu « gélose Chocolat »). Cependant, les milieux Müller-Hinton (MH) ou le milieu écouvillon avec gel Amies Charcoal peuvent également être utilisés. Le milieu de transport doit être ensemencé largement avec une culture pure de 18 à 24 heures maximum et incubé une nuit à 37°C dans une atmosphère enrichie en 5% CO2 avant d’être acheminé au CNRMHi à température ambiante.
ENVOI DU MATÉRIEL BIOLOGIQUE
Tous les prélèvements ou souches à analyser sont à adresser au CNR des Méningocoques et Haemophilus influenzae à l’adresse suivante :
Centre National de Référence des Méningocoques et Haemophilus influenzae
Institut Pasteur 25-28 rue du Docteur Roux 75724 Paris Cedex 15 France
Secrétariat du CNR : 01 45 68 81 78
Téléphone des responsables du CNR : 01 45 68 84 38 / 01 44 38 95 90
Email : meningo@pasteur.fr
Etiquette à compléter et à coller sur l'emballage extérieur (PDF - 20 Ko)
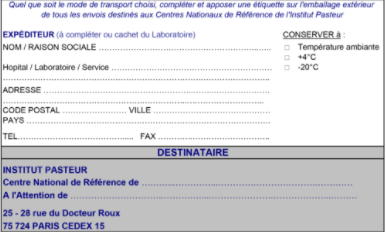
Législation : Tout transport de matériels biologiques potentiellement infectieux demeure sous l’entière responsabilité de l’expéditeur. Les modalités de transport des matières infectieuses sont fixées par l’arrêté français du 5 août 2009 modifiant l'arrêté du 29 mai 2009 relatif au transport des marchandises dangereuses par voies terrestres (dit « arrêté TMD »). Il est recommandé de suivre le Guide sur la sécurité du transport des matières infectieuses et des échantillons de diagnostic publié par l'OMS.
Pour les modalités d’envoi, prendre contact directement avec le laboratoire auparavant.
Emballages et consignes de sécurité :
Les cas de contaminations au laboratoire durant la manipulation de méningocoque et d’Haemophilus influenzae étant rares mais graves, il est indispensable de les prévenir par des précautions de sécurité.
L’envoi, qu’il soit postal ou effectué par un porteur, doit respecter la réglementation pour le transport des matières infectieuses qui tiennent compte de la sécurité des personnes qui expédient, transportent et reçoivent le colis.
- Utiliser un dispositif de sécurité.
- Le transport doit être rapide et sûr (moins de deux jours pour garantir une bonne survie des bactéries).
PRESTATION DE CONSEIL, SUGGESTION ET RÉCLAMATION
Contacter le CNR des Méningocoques et Haemophilus influenzae :
Dr Muhamed-Kheir TAHA - Tél :(+33) 1 45 68 84 38.
Dr Ala-Eddine DEGHMANE - Tél : (+33) 1 44 38 95 90.
Ou le service de coordination des Centres de référence.
MODALITÉS DE CONSERVATION ET RESTITUTION DES ÉCHANTILLONS BIOLOGIQUES TRAITÉS
Les écouvillons avec gel Amies Charcoal ne sont pas conservés et sont éliminés après la subculture.
Les échantillons biologiques sont conservés après leur purification. Ces échantillons purifiés ainsi que le reste des échantillons primaires (s’il y a lieu) sont conservés pour la durée de vie du CNR.
CONFIDENTIALITÉ ET PROTECTION DES INFORMATIONS
Les fichiers informatisés du CNR sont déclarés à la Commission Informatique et Libertés (CNIL) : Loi n°78-17 du 06 janvier 1978.
Voir aussi :
> Organisation des Centres Nationaux de Référence
> Système du Management de la Qualité des Laboratoires de Référence et d’Expertise
CONDITIONS FINANCIÈRES
Voir aussi :
> Organisation des Centres Nationaux de Référence
> Système du Management de la Qualité des Laboratoires de Référence et d’Expertise
Mis à jour le 12/02/2026

