Sommaire
Dossier - Comprendre notre immunité pour mieux vieillir
Tous différents sur le plan de notre ADN comme sur celui de nos défenses immunitaires
Le projet “Milieu Intérieur” : une étude unique pour décrypter notre immunité
Comprendre - Qu’est-ce que l’épigénétique ?
Le sexe biologique façonne notre immunité
Les quatre grands enseignements concernant le vieillissement
Décrypter les secrets de l’immunité selon l’âge, le sexe et la vaccination
Comprendre - Le single-cell sequencing
Vers l’émergence d’une médecine personnalisée du vieillissement
Le tabagisme laisse des traces durables sur notre système immunitaire
Phénomène naturel qui nous concerne tous, le vieillissement ne se limite pas à une simple accumulation d’années. Avec l’augmentation de l’espérance de vie, notamment dans les pays industrialisés, la question de la qualité de ce vieillissement devient centrale. Aujourd’hui, près de 10 % de la population européenne aura plus de 80 ans d’ici 2050, et le nombre de centenaires devrait être multiplié par 18 par rapport à l’an 2000. Cette évolution soulève des enjeux majeurs médicaux et sociaux.
Tous différents sur le plan de notre ADN comme sur celui de nos défenses immunitaires
Si le vieillissement est universel, il ne s’exprime jamais de manière uniforme. Chaque individu possède un patrimoine immunitaire unique, hérité de ses ancêtres, qui influence profondément le fonctionnement de son organisme. Le système immunitaire garde aussi la mémoire des pathogènes contre lesquels il nous a protégés. Sa composition, son efficacité et sa capacité d’adaptation varient considérablement d’une personne à l’autre.
À cette diversité génétique s’ajoutent des différences liées au sexe biologique. Les femmes et les hommes ne disposent pas des mêmes défenses immunitaires ni des mêmes trajectoires de vieillissement. Les femmes présentent en général une réponse immunitaire plus robuste, mais sont également plus exposées à certaines maladies auto-immunes. Les hommes, quant à eux, connaissent un déclin immunitaire parfois plus précoce ou plus marqué, avec des conséquences spécifiques sur la santé à long terme.

“LabEx Milieu Intérieur” - Une recherche française de très grande envergure pour comprendre la variabilité de la réponse immunitaire
C’est précisément pour mieux comprendre cette diversité que le programme “LabEx Milieu Intérieur” a été lancé. Ce vaste projet de recherche français, réunissant 45 laboratoires, s’est donné pour ambition de définir ce qu’est un système immunitaire “sain” et d’en mesurer la variabilité naturelle au sein d’une cohorte de 1 000 adultes non malades (voir encadré page précédente).
En 2021, dix ans après le lancement du programme, la même cohorte est de nouveau étudiée. Cette approche longitudinale offre une opportunité rare : observer comment le système immunitaire évolue au fil du temps chez des individus initialement en bonne santé.
Et ainsi mieux comprendre les mécanismes complexes qui relient le vieillissement et le système immunitaire. Ils montrent d’abord que le vieillissement immunitaire n’est ni linéaire ni uniforme. Il repose sur l’interaction de plusieurs phénomènes biologiques qui évoluent à des rythmes différents selon les individus.
Lancé en 2011 à l’Institut Pasteur et dirigé par Darragh Duffy et Lluis Quintana-Murci, le projet “Milieu Intérieur” étudie la variabilité du système immunitaire chez des individus sains. Contrairement aux recherches ciblées sur des pathologies, il suit une cohorte de 1 000 volontaires – 500 femmes et 500 hommes, âgés de 20 à 70 ans – sur plus de dix ans, combinant analyses génétiques, immunitaires et données environnementales. Cette approche a permis d’identifier des marqueurs prédictifs de maladies, des différences immunitaires liées au sexe ou à l’âge, ainsi que l’impact de facteurs comme le tabagisme ou les infections virales.
Les résultats ouvrent des perspectives pour une médecine plus personnalisée : adaptation des traitements (comme pour la tuberculose), détection précoce de complications métaboliques, ou encore compréhension des mécanismes du vieillissement. Le projet approfondit désormais les liens entre immunité, vieillissement et épigénétique.
En rendant ses données accessibles à la communauté scientifique, Le projet “Milieu Intérieur” contribue à façonner l’avenir de la santé, où prévention et précision deviennent centrales.
Qu'est-ce que l'épigénétique ?
L’épigénétique étudie les modifications réversibles et héritables influençant l’activité des gènes, sans pour autant altérer la séquence de l’ADN elle-même. Elle explore comment des facteurs externes, comme l’environnement, le mode de vie, l’alimentation ou le stress, peuvent activer ou désactiver l’expression de certains gènes, à la manière d’un interrupteur. Ces modifications épigénétiques jouent un rôle crucial dans le développement des organismes et leur adaptation à leur environnement.
Le sexe biologique façonne notre immunité
Les différences entre femmes et hommes face aux maladies sont frappantes : à titre d’exemple, 50 % des femmes subiront une infection urinaire au cours de leur vie, contre seulement 10 à 15 % des hommes. À l’inverse, le cancer de la vessie touche trois fois plus d’hommes, mais les femmes, lorsqu’elles en sont atteintes, sont souvent diagnostiquées à un stade plus avancé et présentent un pronostic plus sévère. Ces disparités soulèvent une question fondamentale : pourquoi les réponses immunitaires et les trajectoires de santé diffèrent-elles selon le sexe ?
L’équipe de Molly Ingersoll s’attaque précisément à cette énigme en étudiant les sites muqueux sous-explorés comme la vessie. Leur hypothèse repose sur l’influence des hormones stéroïdiennes (oestrogènes, progestérone, androgènes cortisol), qui agissent comme des modulateurs puissants du système immunitaire. Pour y répondre, l’équipe a collaboré avec le consortium “Milieu Intérieur” et a analysé 17 hormones différentes dans le sang des volontaires de la cohorte, dont environ 500 sont revenus pour fournir à nouveau des échantillons dix ans plus tard.
"Les femmes et les hommes n'ont pas la même immunité" - Molly Ingersoll, chercheuse à l'Institut Pasteur et l'Institut Cochin, reponsable de l'unité Inflammation et immunité des muqueusesCe suivi longitudinal permet de comprendre l’évolution hormonale au fil du vieillissement. Leurs résultats sont révélateurs.
La contraception hormonale féminine modifie presque tout le paysage stéroïdien, y compris le cortisol et la cortisone, ces régulateurs du stress et de l’immunité. Un impact systémique méconnu qui interroge sur les effets à long terme sur le métabolisme et la résistance aux infections ou autres maladies.
La ménopause se révèle un tournant critique : la chute rapide des oestrogènes et de la progestérone est associée à une susceptibilité accrue aux infections de la vessie et à des changements dans les caractéristiques tumorales des cancers de la vessie.
Chez les hommes fumeurs, une corrélation inattendue apparaît entre tabagisme et androgènes, inexistante chez les femmes, révélant une relation entre les niveaux spécifiques d’hormones mâles et les perturbateurs environnementaux.
Enfin, le suivi sur dix ans montre qu’une baisse marquée des progestagènes est, étonnamment, associée à un risque accru de pathologies uniquement chez les donneurs masculins.
Cette étude a ses limites : elle établit des corrélations, pas des causalités. Mais sa force réside dans la qualité des sets de données, et dans son caractère, rare et précieux.
Les données serviront de référence mondiale. Les projets futurs visent à dissocier les effets des hormones de ceux des chromosomes X/Y et à personnaliser les traitements selon le sexe. L’enjeu est d’adapter la médecine à la biologie réelle des femmes et des hommes, pour des soins plus justes et efficaces pour tout le monde.

L’ADN ancien agit comme un microscope temporel pour observer comment les populations humaines ont réagi aux pathogènes au fil des millénaires.
Le projet “Milieu Intérieur” est une aventure scientifique unique. Quel est votre rôle au sein de ce projet ?
“Milieu Intérieur” est un projet ambitieux qui vise à comprendre la variabilité du système immunitaire humain, en intégrant des données immunologiques, génétiques, épigénétiques et environnementales. Nous visons à identifier les principaux facteurs génétiques et environnementaux affectant la variation de la réponse immunitaire dans la population générale française. Au sein du consortium, je cherche à déterminer les causes du vieillissement immunitaire, et à mieux comprendre comment les altérations de l’ADN influencent la réponse immunitaire avec l’âge. Je coordonne aussi les analyses et la gestion des très grands volumes de données générés par le programme, en m’assurant que les résultats soient robustes et exploitables.
En quoi le séquençage de l’ADN ancien révolutionne-t-il la compréhension du système immunitaire ?
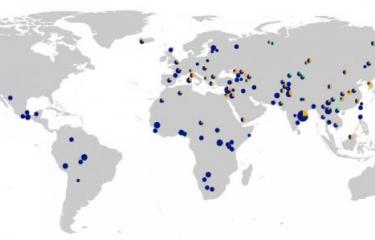
Pour les généticiens, le séquençage de l’ADN ancien équivaut à la découvertedu microscope en microbiologie. Nous pouvons désormais observer directement comment les populations humaines et leurs pathogènes ont évolué au fil des millénaires, plutôt que de nous fier à des modèles théoriques. Cette approche révèle les causes des pandémies historiques comme la peste noire. En comparant les génomes de victimes et survivants enterrés à Toulouse aux XIVe-XVe siècles, nous avons constaté que plusieurs gènes suspectés dans la susceptibilité à la peste ne semblent pas impliqués. Cela suggère que des facteurs non génétiques (nutrition, conditions de vie) ont joué un rôle clé dans cette pandémie qui a tué 30 à 60 % de la population européenne.
L’agriculture a-t-elle vraiment été le tournant majeur pour l’évolution du système immunitaire humain ?
En science, certaines hypothèses plausibles, comme celle de la transition épidémiologique liée à l’agriculture, deviennent des dogmes. Pourtant, nos données montrent que l’âge du bronze a été bien plus déterminant pour le système immunitaire en Europe. Cela s’explique par l’urbanisation, les migrations massives, et l’augmentation de la taille des populations, qui ont favorisé la propagation des agents pathogènes et rendu la sélection naturelle plus efficace. Réévaluer ces théories est crucial pour mieux comprendre les causes des crises démographiques qui ont jalonné l’histoire de notre espèce, et les mécanismes évolutifs qui ont façonné notre immunité.
Vous travaillez aussi sur des populations polynésiennes. Quels enseignements tirez-vous de ces études, notamment sur les maladies métaboliques ?
Avec mes collègues Lluis Quintana-Murci et Van-Mai Cao-Lormeau, nous avons séquencé 1 800 génomes modernes pour étudier l’histoire du peuplement et la susceptibilité aux maladies métaboliques. Contrairement à une idée reçue, nos résultats ne soutiennent pas que l’épidémie d’obésité actuelle est due à un risque génétique accru des populations du Pacifique. Elle est clairement liée à des facteurs environnementaux récents, comme le changement brutal de régime alimentaire. Les Polynésiens consomment aujourd’hui des produits ultratransformés, et leur taux d’obésité est passé de 0 % dans les années 1950 à 50 % aujourd’hui. Ce résultat interroge l’impact des interactions entre gènes et environnement dans les maladies modernes.
Vos recherches montrent que les mutations favorisant la résistance aux infections augmentent aussi le risque de maladies auto-immunes. Comment expliquez-vous ce paradoxe ?
Ce paradoxe n’en est plus un lorsqu’on le comprend à la lumière de la théorie de l’évolution : les mutations qui nous ont protégées des infections peuvent, dans un environnement moins infectieux, devenir délétères. Par exemple, une mutation du gène TLR1, qui augmente la résistance aux pathogènes, est aussi associée à un risque accru d’allergies et d’asthme. Dans un environnement hygiéniste, comme le nôtre, ces mutations ne confèrent plus d’avantage sélectif et peuvent même favoriser les maladies auto-immunes. Ce phénomène pourrait contribuer à la fréquence des allergies et des maladies auto-immunes dans les sociétés modernes.
Quels sont les défis futurs pour votre recherche ?
Pour mieux comprendre l’histoire de notre santé, nous devons développer de nouvelles approches pour retracer les causes de décès de nos ancêtres, comme estimer l’âge au décès à partir de l’ADN ancien, en utilisant des marqueurs liés au vieillissement. Nous souhaitons aussi étudier d’autres épidémies, comme celles qui ont emporté jusqu’à 90 % des populations polynésiennes à l’arrivée des Européens, ou encore la variole ou la grippe espagnole, même si cela pose des défis techniques (le génome viral ancien est difficile à séquencer) et éthiques (les descendants d’individus décédés récemment sont identifiables). Chaque squelette ancien est une pièce du puzzle de notre histoire biologique. Notre santé est le fruit d’une histoire complexe, où gènes et environnement s’entremêlent.
Les quatre grands enseignements concernant le vieillissement
L’un des constats majeurs concerne l’installation progressive d’une inflammation chronique de bas grade (ou inflamm’aging ). Cette inflammation diffuse, peu perceptible cliniquement, s’installe avec l’âge et entretient un terrain favorable au développement de nombreuses pathologies chroniques, telles que les maladies cardiovasculaires, le diabète de type 2 ou certaines maladies neurodégénératives. Elle agit également comme un facteur d’épuisement du système immunitaire, en sollicitant en permanence les défenses de l’organisme.
Les maladies auto-immunes constituent un autre enseignement important. En vieillissant, le système immunitaire peut se dérégler et devenir moins capable de faire la différence entre ce qui appartient à notre organisme et ce qui lui est réellement étranger, comme les virus ou les bactéries. Il arrive alors qu’il attaque par erreur des cellules saines, provoquant des inflammations inutiles. Ces erreurs de fonctionnement favorisent l’apparition ou l’aggravation de maladies dites auto-immunes, dont la fréquence et l’intensité varient selon les personnes, en particulier en fonction du sexe et de l’hérédité.
Les infections virales persistantes, en particulier celles dues à des virus de la famille de l’herpès, comme le cytomégalovirus, jouent également un rôle clé. Ces virus, capables de rester latents pendant des décennies mobilisent durablement les cellules immunitaires chargées de les contrôler. À long terme, cette mobilisation constante contribue à l’appauvrissement du réservoir de cellules immunitaires capables de répondre à de nouveaux agents infectieux.
Enfin, le concept d’horloge épigénétique apporte un éclairage nouveau sur le vieillissement. Il montre que l’âge chronologique ne reflète pas toujours l’état réel de nos cellules. Des facteurs environnementaux, comportementaux ou infectieux peuvent accélérer ou ralentir le vieillissement biologique. L’horloge épigénétique devient ainsi un outil prometteur pour évaluer la trajectoire individuelle du vieillissement immunitaire et anticiper les risques de maladies liées à l’âge. Celle-ci permet d’estimer l’âge biologique réel des cellules, indépendamment de l’âge chronologique.
Deux personnes du même âge peuvent ainsi présenter un vieillissement cellulaire très différent, en fonction de facteurs génétiques, environnementaux ou comportementaux. Cette horloge offre un outil précieux pour anticiper l’évolution du système immunitaire et identifier les leviers d’action possibles.
Décrypter les secrets de l’immunité selon l’âge, le sexe et la vaccination
Notre système immunitaire n’est pas statique : il évolue tout au long de la vie, façonné par des facteurs comme l’âge, le sexe ou l’histoire vaccinale. Grâce à des technologies de pointe comme le single-cell sequencing, ces variations peuvent être analysées, révélant les mécanismes du déclin immunitaire lié à l’âge.
Le single-cell sequencing
Le séquençage de cellule unique (single-cell sequencing) est une technologie de pointe analysant l’ARN cellule par cellule, révélant leur diversité et leur fonctionnement individuel. Grâce à des systèmes microfluidiques, elle identifie des sous-populations cellulaires – comme des cellules tumorales résistantes aux traitements – ou des sous-populations rares apparaissant avec l’âge indétectables par les méthodes classiques. En oncologie, elle permet de distinguer les cellules saines des cellules malignes et d’affiner les cibles thérapeutiques. Cette approche révolutionne les diagnostics, les traitements personnalisés et la compréhension des maladies.
En exposant in vitro les cellules sanguines de 380 individus de la cohorte “Milieu Intérieur” à des pathogènes comme le SARS-CoV-2 ou le virus de la grippe, il a été démontré que les personnes âgées présentent une réponse immunitaire affaiblie, notamment en raison d’une production réduite d’interféron alpha, une protéine cruciale pour bloquer la réplication virale. « Parallèlement, l’analyse de l’ensemble des gènes montre que les lymphocytes T CD4 sont le type cellulaire le plus impacté par l’âge », complète le chercheur.
Leurs travaux confirment également que les femmes bénéficient d’une réponse immunitaire plus robuste que les hommes, un paradoxe connu sous le nom de mortality-morbidity paradox : bien qu’elles vivent en moyenne plus longtemps, elles sont aussi plus sujettes aux maladies auto-immunes. « Chez les femmes, les cellules immunitaires innées, comme les cellules myéloïdes, réagissent plus vigoureusement aux virus, avec une expression accrue de gènes proinflammatoires», précise le chercheur. Cette supériorité s’explique en partie par leurs deux chromosomes X : certains gènes échappent à l’inactivation du second chromosome X, leur offrant un avantage immunologique.
À l’inverse, les hommes âgés de plus de 60 ans perdent souvent leur chromosome Y (jusqu’à 50 % dans certains cas), un phénomène que l’équipe a associé pour la première fois à une réponse immunitaire affaiblie. « Cette perte pourrait expliquer pourquoi les hommes sont plus vulnérables aux infections sévères en vieillissant », souligne Marwan Sharawy. Ces découvertes ouvrent des perspectives prometteuses pour préserver une immunité robuste malgré l’âge. « Si nous parvenons à comprendre pourquoi certaines personnes âgées conservent un système immunitaire performant, nous pourrons peut-être reproduire ces conditions chez d’autres », espère Marwan Sharawy. Ses résultats pourraient inspirer de nouvelles approches thérapeutiques, comme la stimulation ciblée de l’interféron alpha. « L’objectif n’est pas seulement de vivre plus longtemps, mais de vieillir en meilleure santé », résume-t-il.

Vers l’émergence d’une médecine personnalisée du vieillissement
L’ensemble de ces observations converge vers un constat clair : une approche uniforme de la santé ne suffit plus face à la diversité des profils immunitaires et des trajectoires de vieillissement. Comprendre le vieillissement implique désormais de tenir compte de l’âge biologique, du patrimoine génétique, de l’histoire infectieuse et du mode de vie de chaque individu.
Cette prise de conscience ouvre la voie à une médecine plus personnalisée, fondée sur l’identification de biomarqueurs précis. Ces marqueurs permettent d’évaluer l’état du système immunitaire, de détecter précocement les déséquilibres et d’adapter les stratégies de prévention et de prise en charge. Il devient ainsi possible de proposer des calendriers vaccinaux adaptés, de cibler plus efficacement les infections virales persistantes ou de mettre en place des actions spécifiques pour limiter l’inflammation chronique.
Au-delà de la prévention, cette médecine personnalisée vise également à optimiser les traitements, en tenant compte des caractéristiques propres à chaque patient. L’objectif est double : améliorer l’efficacité des interventions médicales et réduire les effets indésirables, tout en accompagnant chacun vers un vieillissement en meilleure santé. Face à la diversité des profils immunitaires et des trajectoires de vieillissement, la médecine doit devenir plus personnalisée et proposer des stratégies sur mesure : optimisation des vaccins, recommandations nutritionnelles personnalisées ou ajustements ciblés du mode de vie. Mais les innovations ne s’arrêtent pas là : des pistes thérapeutiques prometteuses émergent, telles que la thérapie génique ou les interventions sur l’épigénétique, qui pourraient un jour permettre de “rembobiner” notre horloge biologique. En ciblant l’inflammation chronique ou en stimulant la régénération des cellules immunitaires, ces approches pourraient prolonger notre santé, bien au-delà de la simple longévité.
Le tabagisme laisse des traces durables sur notre système immunitaire
Le tabagisme laisse une empreinte durable sur le système immunitaire, jusqu’à 40 ans après l’arrêt. La cigarette influence nos défenses aussi profondément que l’âge ou le sexe, en modifiant la production de cytokines, protéines clés de la réponse immunitaire.
Cette empreinte persiste grâce à des modifications épigénétiques – des altérations de l’expression génique sans changement de l’ADN – affectant des immunomodulateurs. Ainsi, pour certaines réponses immunes, les anciens fumeurs conservent un profil immunitaire proche de celui des fumeurs actifs, malgré des années d’abstinence. Le message est clair : il n’est jamais trop tard pour arrêter de fumer, même si le mieux est de ne pas commencer.
L’analyse de la cohorte “Milieu Intérieur” a également révélé deux autres facteurs influençant fortement notre système immunitaire. Le premier est le cytomégalovirus humain (CMVH), un virus très courant qui modifie durablement certaines cellules immunitaires. Le second est le surpoids : un indice de masse corporelle (IMC) élevé perturbe en effet la production de messagers immunitaires importants, comme l’interleukine-2. Pour isoler ces effets, les chercheurs ont stimulé des cellules sanguines avec des agents pathogènes et croisé les résultats avec 136 variables (sociodémographiques, habitudes de vies, etc.). Des analyses statistiques avancées ont confirmé que le tabagisme, le CMVH et l’IMC influencent l’immunité indépendamment de l’âge et du sexe, avec des altérations persistantes de l’ADN chez les anciens fumeurs.

Ces découvertes ouvrent des perspectives majeures pour la santé publique. L’équipe étudie désormais l’influence de l’exposome (ensemble de tout ce à quoi nous sommes exposés dans notre vie : pollution, alimentation, stress, produits chimiques, virus, etc.) sur l’immunité et cherche à identifier les voies métaboliques et épigénétiques impliquées. « Comprendre comment notre environnement façonne notre immunité permettra des stratégies de prévention plus ciblées », souligne Violaine Saint-André. « L’expression de nos gènes est très régulée », résume la chercheuse.
Nos choix et notre environnement comptent, et identifier les leviers adaptés, arrêt du tabac, alimentation équilibrée, permet à chacun d’influencer son capital santé.
Vivre plus longtemps… en pleine santé
L’alliance entre prévention, personnalisation et interventions ciblées dessine l’avenir de la prise en charge du vieillissement. Les traitements antiinflammatoires ou antiviraux en développement, combinés à une meilleure compréhension de notre ADN, pourraient révolutionner la qualité de vie des seniors. Non seulement vivre plus longtemps, mais surtout vieillir en pleine santé, avec un système immunitaire résilient et un organisme mieux armé contre les maladies liées à l’âge.