Les analyses moléculaires ont révélé que la génétique joue un rôle important dans ce que l’on appelle désormais les troubles du spectre autistique (voir notre fiche dédiée). Cette connaissance ouvre de nouvelles pistes pour la prise en charge des personnes avec autisme.
C’est en 1943 que l’autisme a été décrit pour la première fois par un pédopsychiatre américain d’origine autrichienne, Leo Kanner, alors qu’il suivait onze enfants depuis plusieurs années. Dès lors, le débat sur l’origine de l’autisme n’a cessé parmi les spécialistes : naît-on autiste ou le devient-on ? Longtemps, la piste « acquise » a prévalu. Mais soixante ans après la description de Leo Kanner, c’est dans l’Hexagone que pour la première fois des mutations génétiques ont été identifiées : une découverte réalisée à l’Institut Pasteur par l’unité Génétique humaine et fonctions cognitives de Thomas Bourgeron, en collaboration avec des psychiatres français (Marion Leboyer) et suédois (Christopher Gillberg). Aujourd’hui, plus personne ne conteste que l’autisme a une composante génétique très forte.
Quelques dates clés sur l'autisme
- 1911 : Pour la première fois, le terme « autiste » apparaît dans un traité de psychiatrie. Il est associé à la schizophrénie
- 1943 : Le pédopsychiatre américain Leo Kanner dresse le tableau clinique de l’autisme infantile précoce
- 1944 : Le pédopsychiatre autrichien Hans Asperger utilise le terme « autisme » pour décrire des patients avec des troubles de l’interaction sociale mais sans atteintes du langage et des fonctions cognitives
- 1950-1960 : Le psychanalyste américain Bruno Bettelheim émet l’hypothèse que le comportement de certaines mères « réfrigérateurs » serait à l’origine de l’autisme de leur enfant
- 1960-1970 : Pour la plupart des experts, l’autisme est une psychose, une maladie mentale acquise qui doit être traitée par la psychanalyse
- 1970-1980 : Des chercheurs américains et français utilisent l’encéphalographie et émettent l’hypothèse que l’autisme serait lié à des troubles précoces de la perception sensorielle. De plus en plus d’études s’intéressent à l’autisme chez les jumeaux ou chez des enfants apparentés. Ces études révèlent la contribution important de la génétique.
- 2001 : Un rapport américain conclut que des programmes d’éducation individualisés sont la meilleure prise en charge pour les autistes. En France, les traitements psychothérapeutiques restent encore privilégiés
- 2003 : Pour la première fois, des mutations génétiques sont identifiées précisément chez des enfants autistes, par l’équipe de Thomas Bourgeron à l’Institut Pasteur en collaboration avec des psychiatres français (Pr Marion Leboyer) et suédois (Pr Christopher Gillberg). D’autres mutations seront mises au jour ensuite
- 2005-2007 : 1er plan autisme en France
- 2008 : Création des premiers modèles animaux porteurs de mutations associées à un trouble du spectre autistique (TSA)
- 2008-2010 : 2e plan autisme
- 2012-2018 : Projet EU-AIMS
- 2013 : Nouvelle version du DSM-5 (manuel diagnostique et statistique des troubles mentaux) avec l’utilisation du diagnostic de trouble du spectre autistique
- 2013-2017 : 3e plan autisme (dépistage précoce la scolarisation des enfants TSA)
- 2018-2024 : Projet AIMS-2-Trials
- 2018-2022 : 4e plan autisme
- 2019 : La liste officielle SPARK dénombre 141 gènes associés à l’autisme.
Un ensemble de troubles complexes
L’autisme est caractérisé par deux types de symptômes, qui s’expriment à des degrés variables selon les individus : troubles de la communication sociale et troubles du comportement qui correspondent à un répertoire restreint d’intérêts et d’activités, avec notamment des gestes stéréotypés (battre des mains, se balancer, tourner sur soi-même, faire des mouvements complexes avec son corps…). Ces signes peuvent s’accompagner d’une hypersensibilité ou au contraire d’une hyposensibilité sensorielle (sons, lumière, toucher…) et d’une forte émotivité face à tout changement dans l’environnement. L’autisme est très souvent accompagné d’autres signes cliniques comme la déficience intellectuelle, l’hyperactivité, des troubles du sommeil, des troubles alimentaires ou l’épilepsie. Cette description a été élargie, et l’on préfère parler plus globalement des troubles du spectre autistique (ou TSA) qui incluent d’autres formes d’autisme comme le syndrome d’Asperger, où le langage n’est pas atteint et la personne présente un quotient intellectuel dans la norme ou plus élevé que la moyenne.
L'autisme en chiffres
- Plus d'une personne sur 100 serait concernée par un trouble du spectre autistique (TSA)
- Plus de 650 000 personnes sont concernées par un TSA, en France
- Plus de 140 gènes ont été identifiées à ce jour associés à l’autisme
- Dans 20-30 % des cas, la cause de l’autisme est associée à un gène connu. Plus la recherche avance, plus le nombre de gènes découverts augmente. Ces gènes peuvent avoir un lien direct avec l’autisme ou indirect via des symptomes associés comme la déficience intellectuelle.
C’est dans la petite enfance que les premiers signes apparaissent, en général avant l’âge de 3 ans. Dans la grande majorité des cas, ils se maintiennent ensuite durant toute la vie. Si l’on considère l’ensemble des TSA, les garçons sont 4 à 8 fois plus touchés que les filles. Par ailleurs, certaines formes de TSA sont directement associées à des maladies génétiques telles que le syndrome de l’X fragile ou le syndrome de Rett.
En France, on estime que plus de 650 000 personnes sont touchées par un trouble autistique. Aux États-Unis, d’après le Center of Diseases Control, c’est plus d’une personne sur 100 qui est concernée par un trouble autistique. L‘augmentation de la prévalence de l’autisme s’explique à la fois par l’élargissement des critères diagnostiques et par une meilleure détection des personnes avec autisme.
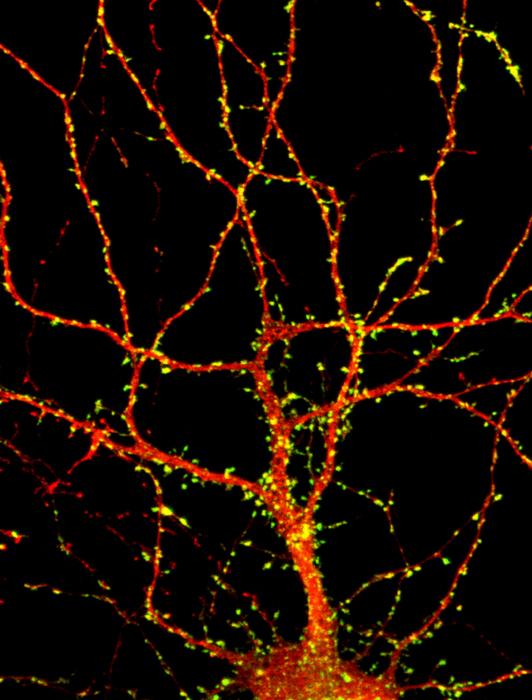
La piste d'une origine génétique
Les experts sont aujourd’hui unanimes pour reconnaître une forte implication de facteurs génétiques. Dès les années 1970, des recherches sur des jumeaux et plus largement sur des familles, ont en effet révélé la piste génétique dans la survenue de l’autisme. Depuis de nombreuses études ont montré que lorsqu’un enfant était autiste, son jumeau l’était aussi dans 98 % des cas s’il s’agissait d’un jumeau monozygote (c’est-à-dire possédant exactement le même patrimoine génétique, « vrai jumeau ») et dans environ 50 % s’il était jumeau dizygote (« faux jumeau »).
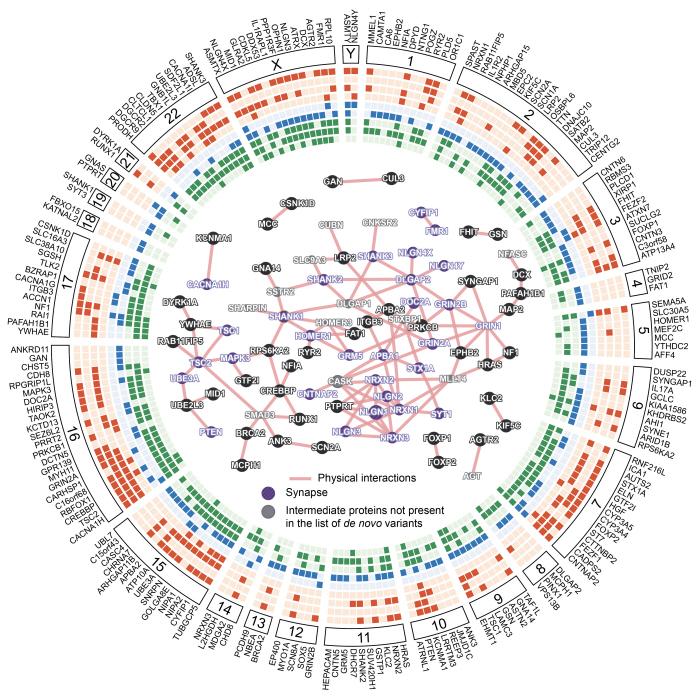
Mais pour comprendre réellement les mécanismes génétiques de l’autisme, et même identifier des mutations impliquées, il a fallu attendre le début des années 2000 et l’avènement des techniques de biologie moléculaire et de séquençage. C’est en 2003 que l’équipe de Thomas Bourgeron à l’Institut Pasteur identifie pour la première fois des mutations sur deux gènes présents sur le chromosome X chez deux frères l’un diagnostiqué autiste et l’autre avec un syndrome d’Asperger. Ces mutations affectent des gènes directement impliqués dans le fonctionnement des points de contact entre les neurones aussi appelés synapses. Pour la première fois donc, un lien est établi entre mutation génétique, fonctionnement des synapses et troubles du spectre autistique. Quatre ans plus tard, la même équipe identifie un autre gène, impliqué cette fois dans la structure même des synapses. Ces résultats ont confirmé la « voie synaptique » dans l’étiologie de l’autisme, et ils seront corroborés par la suite par des études internationales effectuées sur de plus grands nombres de personnes avec autisme. En 2008, ces mêmes chercheurs de l’Institut Pasteur découvrent chez certaines personnes avec autisme une mutation sur un gène impliqué dans la synthèse de la mélatonine. Cette hormone joue un rôle central dans la régulation des rythmes biologiques, notamment le sommeil. Or chez de nombreux enfants avec autisme, on retrouve un déficit en mélatonine qui expliquerait en partie les troubles du sommeil présents chez environ 60 % d’entre eux. Un déficit en mélatonine d’origine génétique constituerait donc un autre facteur de risque d’autisme.
La base de données la plus complète au monde hébergée à l'Institut Pasteur
L’Institut Pasteur héberge la plus grande base de données au monde sur l’autisme, non pas en nombre de patients – 800 actuellement et jusqu’à 3 000 à terme – mais en quantité et richesse d’informations recueillies pour chacun : imagerie cérébrale, électro-encéphalogrammes, données génomiques, profils psychologiques, quotient intellectuel, qualité de vie, tests comportementaux, etc. « Comparée aux bases de données existantes pour l’autisme, c’est de la “haute-couture” », souligne Thomas Bourgeron, responsable de l’unité de Génétique humaine et fonctions cognitives à l’Institut Pasteur, pionnier dans la découverte et l’étude des gènes associés à l’autisme.

Ce chercheur coordonne le volet génétique du programme européen AIMS-2-Trials* impliquant 106 sites dans 37 pays d’Europe pour la recherche de nouvelles prise en charge de l’autisme, grâce auquel ces multiples données ont été réunies. Dans son équipe, Guillaume Dumas précise : « L’élaboration de cette base de données est un défi technique, qui obéit aussi aux règles éthiques très strictes qui encadrent l’accès et la sécurisation des données de santé des personnes. Nous travaillons avec la Direction déléguée aux systèmes d’information (DSI) pour stocker et organiser le « rangement » de ces données, et avec des biostatisticiens du Centre de bioinformatique pour développer des outils pour leur analyse et faciliter l’accès des informations aux chercheurs.»
Ce spécialiste des ondes cérébrales rappelle qu’il y a peu, il travaillait « avec de gros classeurs à l’hôpital conten Autism Innovative Medicine Studies-2-Trialsant des centaines de DVD gravés d’électro-encéphalogrammes des patients » ! La centralisation de toutes les données numérisées dans la nouvelle base EU-AIMS, disponible via Internet aux scientifiques du monde entier, va permettre aux chercheurs, depuis leurs ordinateurs, de croiser une multitude d’informations pour lancer des analyses robustes et reproductibles qui vont sans aucun doute accélérer à vitesse grand V la compréhension de l’autisme. Et, c’est l’objectif, aboutir à des prises en charge adaptées aux différents types d’autisme et aux caractéristiques de chaque patient. L’enjeu est de taille : rappelons que les « troubles du spectre autistique » concernent plus de 1% de la population.
*Autism Innovative Medicine Studies-2-Trials
De multiples facteurs impliqués
Depuis, et grâce aux travaux de diverses équipes dans le monde, d’autres mutations génétiques ont été identifiées. Le nombre de gènes identifiés dans l’autisme augmente et le plus souvent ils concernent deux processus biologique : la formation du système nerveux en modulant la formation des synapses (la synaptogenèse) et la régulation des gènes.
De fait, il est désormais acquis que des facteurs génétiques jouent un rôle essentiel dans la vulnérabilité à l’autisme. Mais l’extrême variabilité des troubles d’une part, et le grand nombre de mutations découvertes d’autre part, rendent la tâche difficile pour les chercheurs. Si dans certains cas, la variation d’un seul gène peut expliquer une grande partie des symptômes d’un patient, dans d’autres cas la situation génétique est beaucoup plus complexe, impliquant parfois plus d’une centaine de gènes qui individuellement n’auraient pas d’effet, mais qui combinés ensemble, augmentent le risque d’avoir un autisme. Et la situation est d’autant plus complexe que chez 10 à 20 % des personnes, ces mutations génétiques ne sont pas héritées, mais sont apparues de novo (de manière spontanée).

En tant que psychiatre, je travaille surtout sur les symptômes cliniques mais aussi sur le cerveau, ses structures et ses fonctions. En collaborant avec l’Institut Pasteur, j’essaie de mettre en relation ces données avec l’apport génétique. Chaque individu est unique, car il possède un terrain génétique particulier mais également un environnement qui lui est propre.
Quels sont les enjeux majeurs auxquels vous faites face dans votre pratique de psychiatre ?
En tant que pédopsychiatre, je fais face à plusieurs enjeux dans ma pratique. Le premier est l’âge de début du trouble. Il s’agit de comprendre ce qui se passe dans les premiers moments de la vie car le diagnostic actuel à 36 mois est en soit une certaine aberration. Certains enfants présentent des signes beaucoup plus précocement (en moyenne 15 mois) et c’est une véritable souffrance pour les familles. La compréhension précoce des mécanismes est donc essentielle. Comment peut-on enrayer rapidement l’apparition de ces symptômes ? C’est une question fondamentale pour essayer d’améliorer le pronostic et la trajectoire développementale.
Le deuxième enjeu est la question de l’évolution du trouble. Certains enfants présentant des symptômes très sévères ont une évolution très favorable de leur trajectoire développementale et ont des compétences socio-communicationnelles semblables à celles des personnes dites neurotypiques (sans anomalie du développement). Il est donc très important de comprendre les facteurs à l’origine de ce phénomène. Sont-ils biologiques ? Sont-ils le résultat d’une bonne stratégie thérapeutique ? Ce sont des questions auxquelles nous essayons de répondre.
Le troisième enjeu est celui de la compréhension de l’augmentation de la prévalence de l’autisme. C’est une question complexe. Il y a de nombreux facteurs qui concourent à l’augmentation de la prévalence de l’autisme, par exemple l’accrétion diagnostique. C’est-à-dire que plus on connaît l’autisme, plus on donne des diagnostics de l’autisme; L’augmentation de l’âge parental; les modifications des critères diagnostiques ayant permis une certaine versatilité dans le diagnostic des troubles du spectre autistique (en particulier dans sa communalité avec les troubles induisant un déficit intellectuel).
Vers quelles perspectives thérapeutiques êtes-vous en train de vous diriger ?
Nous avons récemment testé plusieurs centaines de molécules très spécialisées pour étudier leur impact sur le gène SHANK3, premier gène de l’autisme qui a été découvert par Thomas Bourgeron. Nous avons observé, sur des neurones issus des patients (transformation par exemple de cellules de la peau d’un patient en neurones), des modifications du taux de SHANK3 après l’administration de ces molécules. Nous avons découvert que certaines molécules comme l’acide valproïque ou le lithium pouvaient augmenter le taux de transcript SHANK3 et par conséquence l’activité neuronale. Mais ces molécules, si elles agissent sur SHANK3, ont un également un impact sur d’autres molécules du corps humain.
Il y a quelques temps, nous avons testé le lithium chez une patiente. Au bout de trois mois, nous avons observé une nette amélioration des capacités d’interaction et de communication verbale et donc une amélioration des scores liés à l’autisme. Par contre, la patiente montrait pourtant des signes d’hyperactivité. Au final, son adaptation au quotidien n’avait pas tellement changé.
Aujourd’hui, ces molécules permettent d’améliorer certains symptômes, même si on ignore encore comment. L’important, c’est que des techniques de pointe permettent d’envisager de nouvelles stratégies thérapeutiques. La nécessité de mise en place d’essais thérapeutiques est plus qu’importante. Il faut conjuguer des efforts économiques et logistiques pour mettre en place des essais cliniques capable de généraliser des résultats observés sporadiquement à travers le monde.
En quoi la collaboration avec l’Institut Pasteur est-elle essentielle pour améliorer la prise en charge des personnes avec autisme ?
J’ai commencé à travailler sur la génétique de l’autisme en collaboration avec l’Institut Pasteur pour comprendre comment améliorer la santé des patients que je reçois à l’hôpital Robert Debré en essayant de comprendre les voies biologiques impliquées dans les maladies de mes patients et ainsi à terme d’envisager d’identifier de nouvelles approches thérapeutiques.
En tant que psychiatre, je travaille surtout sur les symptômes cliniques mais aussi sur le cerveau, ses structures et ses fonctions. En collaborant avec l’Institut Pasteur, j’essaie de mettre en relation ces données avec l’apport génétique. Chaque individu est unique, car il possède un terrain génétique particulier mais également un environnement qui lui est propre.
La découverte des premiers gènes de l’autisme par Thomas Bourgeron a révolutionné la conception de ce trouble en France. Pour la première fois, on a validé une hypothèse biologique et non plus seulement les interactions entre l’enfant et ses parents. Les recherches ont continué, et non seulement les gènes ont été découverts, mais c’est aussi toute l’architecture de la synapse qui a été décortiquée. A l’Institut Pasteur, j’ai appris que de nombreuses protéines à l’intérieur de la synapse pouvaient devenir des cibles thérapeutiques pour améliorer l’ensemble des symptômes. Ce sont des défis que nous essayons de relever au quotidien pour améliorer la qualité de vie des patients.
Vers une médecine personnalisée
Ces découvertes laissent cependant entrevoir de nouvelles pistes de prises en charge pour réduire la sévérité des troubles en particulier les symptômes associés comme la déficience intellectuelle et l’épilepsie. La collaboration étroite entre généticiens, neurobiologistes et psychiatres permet en effet de mieux comprendre le fonctionnement du cerveau, et les conséquences de telle ou telle variation génétique. De sorte que certaines équipes testent d’ores et déjà des prises en charge adaptées en fonction de la mutation génétique identifiée chez un groupe de personnes avec autisme. Ainsi cette approche personnalisée de l’autisme pourrait être une voie d’avenir pour aider chaque individu selon ses besoins et ses particularités.
Une rencontre exceptionnelle à l’Institut Pasteur le 30 mars 2019
L’étroite collaboration entre généticiens, neurologues et psychiatres a été largement illustrée lors de la journée du 30 mars 2019 où experts et patients ont pu se rencontrer. Près de 550 personnes étaient rassemblées à l’Institut Pasteur pour une rencontre exceptionnelle consacrée aux avancées de la recherche sur l’autisme et les troubles qui lui sont associés.
Les derniers travaux et découvertes sur l’autisme issus des interactions entre les chercheurs de l’Institut Pasteur, les pédopsychiatres de l’hôpital Robert-Debré, et plus largement les partenaires français et européens ont été exposés. Surtout, c’est l’importance de la génétique, la nécessité d’un diagnostic précis et précoce et la complexité des traitements du fait de la grande diversité des profils des personnes avec autisme qui ont été évoquées.

Retrouvez, en images, l'intégralité de la conférence "Autisme, que nous enseigne la recherche ?"
L'autisme dans le plan stratégique 2019-2023 de l'Institut Pasteur

L’un des trois axes scientifiques prioritaires du plan stratégique 2019-2023 de l’Institut Pasteur se concentre sur les maladies de la connectivité cérébrale et les maladies neurodégénératives. L’Institut Pasteur cherche possède de nombreuses ses compétences en recherche fondamentale dans les domaines des neurosciences, de la génétique, de la biologie des cellules et du développement, de l’immunologie, de la microbiologie et de la biologie des infections pour appréhender la complexité des fonctions cérébrales. Ces projets portent entre autre sur les troubles neuro-développementaux comme l’autisme. Les recherches en biologie cellulaire s’intéressent à la connectivité neuronale en associant des analyses génomiques et cellulaires, de la microscopie innovante, et de modélisation.
De fait, il est désormais acquis que des facteurs génétiques jouent un rôle essentiel dans la vulnérabilité à l’autisme. Mais l’extrême variabilité des troubles d’une part, et le grand nombre de mutations découvertes d’autre part, rendent la tâche difficile pour les chercheurs. Si dans certains cas, la variation d’un seul gène peut expliquer une grande partie des symptômes d’un patient, dans d’autres cas la situation génétique est beaucoup plus complexe, impliquant parfois plus d’une centaine de gènes qui individuellement n’auraient pas d’effet, mais qui combinés ensemble, augmentent le risque d’avoir un autisme. Et la situation est d’autant plus complexe que chez 10 à 20 % des personnes, ces mutations génétiques ne sont pas héritées, mais sont apparues de novo (de manière spontanée).




